CRISPR, l’ange et le démon
L’ange se disait que
CRISPRdevait devenir son meilleur ami. Même s’il n’avait pas toujours été très fidèle, les « autres », ces technologies obsolètes
d’ingénierie des génomes, ne semblaient plus l’intéresser. CRISPR avait su attirer son attention comme une « fantastique invention » de la nature mise au service des desseins de l’homme. Ses géniteurs mériteraient sûrement un prix Nobel pour cette entité qui semblait parfaite pour les aider à reconstruire le vivant aux fins des biotechnologues. Parfaite, pas tant que cela pensait le démon, qui rêvait déjà d’exploiter toutes les failles que les
lois de la naturesavent aussi créer, pour détourner et mettre à mal les plus belles technologies humaines. Ange et démon sont
deux faces de toute technologie de rupture. Qu’en est-il des différentes approches qui rivalisent actuellement pour éditer les génomes ? [bloc_image]

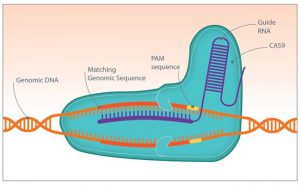
[/bloc_image]
(Crédits images : http://www.genengnews.com/bioperspectives/ & http://www.observatoriobioetica.org)
L’ingénierie ciblée des génomes se place actuellement comme une pierre d’angle des biotechnologies, que la cible soit la production biosourcée de composés chimiques définis, de ressources énergétiques ou alimentaires ou d’applications biomédicales. Quel que soit l’objectif, l’édition d’un génome, qu’il s’agisse d’introduire, de modifier ou de supprimer des gènes, passe par un mécanisme naturel «
la recombinaison» qui exploite en les détournant les capacités naturelles de réparation des organismes. Le problème est que ces
mécanismesnaturels sont d’une part soigneusement
régulés, ce qui les rend parfois inefficaces quand on cherche à les détourner, d’autre part
imparfaits, les erreurs éventuelles conduisant à des modifications génétiques incontrôlées pouvant avoir des conséquences indésirables, voire intolérables par exemple en thérapie génique. Le secret, puisqu’il y en a un, consistait à favoriser et à cibler les mécanismes naturels de recombinaison en ne donnant pas le choix à l’organisme de faire autrement. Pour cela on va d’abord
casser l’ADNdu génome à l’aide d’un outil moléculaire dont la principale caractéristique devra être sa spécificité. Cette
spécificitédoit pouvoir être
ajustée à souhaitpour cibler une séquence unique et choisie à volonté. L’intérêt d’introduire une cassure au sein du génome est qu’une
réparation cibléedevient indispensable à la survie de l’organisme et que la manière la plus facile de la réaliser est de mettre en œuvre un évènement de recombinaison homologue avec un fragment
d’ADN synthétique, qui permettra au passage les modifications génétiques souhaitées. Cela ramène donc le problème à disposer de «
ciseaux moléculaires» spécifiques. De nombreuses technologies (les autres) se sont succédé. Historiquement, l’utilisation d’enzymes naturelles « les
méganucléases» qui reconnaissaient de longues séquences spécifiques d’ADN a d’abord été exploitée. Néanmoins ce système ne permettait pas de choisir facilement le site d’ingénierie qui était prédéfini par la spécificité naturelle de l’enzyme. Dans la génération suivante, les biotechnologues ont su faire « évoluer » ces enzymes naturelles pour leur donner de nouvelles spécificités. Néanmoins, ces chimères étaient longues et complexes à concevoir au cas par cas, et manquaient souvent d’efficacité même si leur spécificité était généralement bonne. Une première rupture est apparue avec le développement de méganucléases modulaires (enzymes à
doigt Zincet
TALENS) dont la spécificité pouvait être dessinée rationnellement en combinant une chaine de modules de reconnaissance à un domaine catalytique de coupure. Ces dernières, en particulier les TALENS étaient plus rapides et beaucoup moins coûteuses à concevoir, mais leur fabrication relevait néanmoins de technologies relativement sophistiquées, peu accessibles directement aux chercheurs qui devaient souvent les faire fabriquer à façon par des sociétés spécialisées. La rupture conceptuelle suivante à conduit aux fameuses CRISPR (formellement
CRISPR-CAS9) où la reconnaissance dépendait non plus d’une protéine mais d’un ARN (guide) qu’il suffisait de changer pour changer à volonté la spécificité. Cet ARN était lui-même exprimé à partir d’un ADN très facile et rapide à synthétiser chimiquement. CRISPR est rapidement apparue comme une technologie nobélisable et «
presque parfaite» pour l’ingénierie des génomes. Néanmoins il faut
relativiser: sa spécificité n’égale souvent pas celle que permettaient les méganucléases ou les TALENS. Par ailleurs ces dernières pouvaient être exploitées en injectant au sein des cellules à transformer non pas un ADN ou/et ARN mais les protéines elles-mêmes, ce qui réduisait d’autant la probabilité
d’évènements parasitesrésultant d’’intégration non souhaitable d’ADN étranger. Par ailleurs, CRISPR, comme les autres nucléases, ne réalise que la
première étape de la recombinaison, laissant ouvert aux « démons naturels » la possibilité d’exploiter toute une collection d’autres évènements parasites lors de la phase de réparation. Il reste donc une grande
marge d’améliorationpossible, en particulier pour des dispositifs qui permettraient de synchroniser coupure et réparation au sein d’un même complexe. Il n’empêche que CRISPR reste actuellement le meilleur outil des «
géno-technologues» en attendant la prochaine étape. Celle-ci pourrait provenir, comme publié très récemment, de l’utilisation d’un complexe de coupure exploitant un guide ADN et non plus un ARN et pour laquelle on nous promet de plus une meilleure spécificité. Il reste que ces nouveaux outils rendent facilement accessible à tous l’ingénierie ciblée des génomes. Cette dernière restera probablement longtemps un champ de bataille majeur entre nos anges et nos démons (et leurs avocats), avec des
aspects éthiquesincontournables si l’on considère par exemple l’ingénierie des cellules souches ou des embryons humains.
Pour en savoir plus
- Article général : https://en.wikipedia.org/wiki/Genome_editing
- TALEN and CRISPR/Cas Genome Editing Systems: Tools of Discovery. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4207558/
- Meganucleases and Other Tools for Targeted Genome Engineering: Perspectives and Challenges for Gene Therapy. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3267165/
- Exploring the potential of genome editing CRISPR-Cas9 technology. Gene. 2016 Nov 8. pii: S0378-1119(16)30886-1. doi: 10.1016/j.gene.2016.11.008.


